- 关于我们
-
全程赋能
产品设计
 产品设计我们凭借15年以上的医疗器械设计制造经验,将您的需求转化为可靠的、分阶段推进的解决方案NPI
产品设计我们凭借15年以上的医疗器械设计制造经验,将您的需求转化为可靠的、分阶段推进的解决方案NPI NPI专业的NPI体系加速产品产业化,确保设计输入100%转化为可靠交付质量管理
NPI专业的NPI体系加速产品产业化,确保设计输入100%转化为可靠交付质量管理 质量管理ISO13485质量体系,全链路零缺陷管控,为每件产品赋予生命线保障项目管理
质量管理ISO13485质量体系,全链路零缺陷管控,为每件产品赋予生命线保障项目管理 项目管理经验丰富的管理团队、敏捷的项目管理,确保您的项目合规、成本、进度三重目标零妥协达成检测能力
项目管理经验丰富的管理团队、敏捷的项目管理,确保您的项目合规、成本、进度三重目标零妥协达成检测能力 检测能力多项检测能力支持产品及工艺验证,如表面性能检测、可靠性测试、生物检测、双酚A检测等临床与注册
检测能力多项检测能力支持产品及工艺验证,如表面性能检测、可靠性测试、生物检测、双酚A检测等临床与注册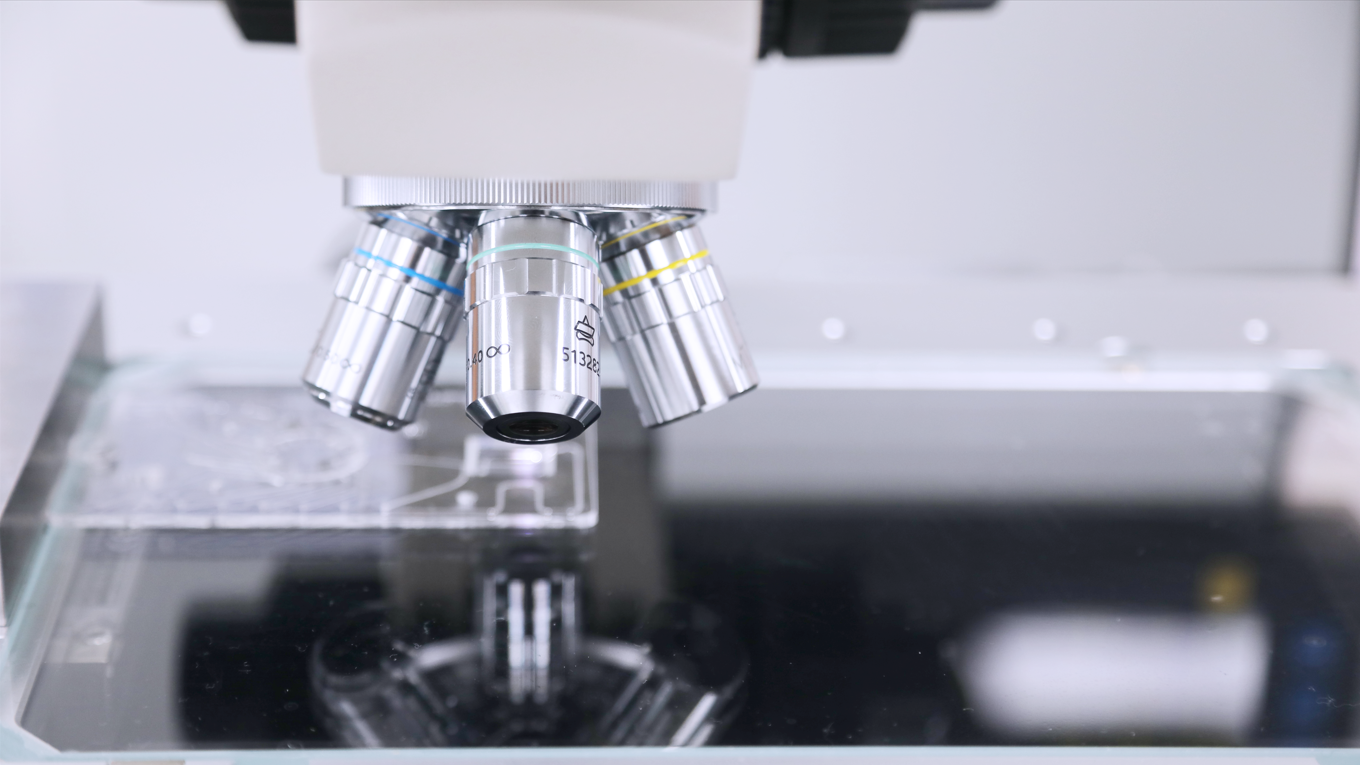 临床与注册提供注册申报服务,协助临床试验支持及技术文件处理,获取CE、FDA认证供应链管理
临床与注册提供注册申报服务,协助临床试验支持及技术文件处理,获取CE、FDA认证供应链管理 供应链管理实施医疗器械专属供应链解决方案:含供应商合规审计、原料批次溯源管理及替代方案验证MAH服务
供应链管理实施医疗器械专属供应链解决方案:含供应商合规审计、原料批次溯源管理及替代方案验证MAH服务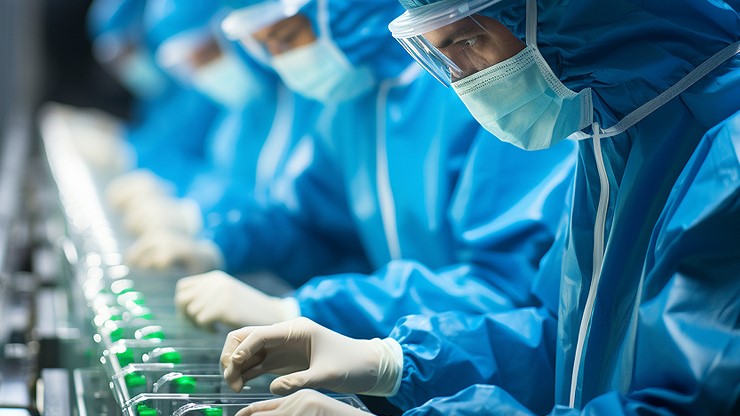 MAH服务依托40万㎡智能化生产基地和专业合规团队,帮助客户实现轻资产运营、快速上市、全球合规
MAH服务依托40万㎡智能化生产基地和专业合规团队,帮助客户实现轻资产运营、快速上市、全球合规 -
技术能力
模具制造
 模具制造精密模具的设计与制造,以微米级精度为核心,助力生产效率与产品质量双提升注拉吹
模具制造精密模具的设计与制造,以微米级精度为核心,助力生产效率与产品质量双提升注拉吹 注拉吹依托一步法注拉吹技术与优质PET材料,专注打造高性能医药包装容器产品挤出与管材
注拉吹依托一步法注拉吹技术与优质PET材料,专注打造高性能医药包装容器产品挤出与管材 挤出与管材凭借丰富的挤出与管材制造经验,打造覆盖从微创介入到智能导管的全套挤出解决方案,以微米级精控重塑导管性能边界传感器集成
挤出与管材凭借丰富的挤出与管材制造经验,打造覆盖从微创介入到智能导管的全套挤出解决方案,以微米级精控重塑导管性能边界传感器集成 传感器集成专业的传感器集成服务,提供温度传感器、磁传感器的设计开发、产品定制化及封装,实现复杂传感器在微创设备微小空间内的高密度、高可靠性集成微组装
传感器集成专业的传感器集成服务,提供温度传感器、磁传感器的设计开发、产品定制化及封装,实现复杂传感器在微创设备微小空间内的高密度、高可靠性集成微组装 微组装复杂装配的解决方案,环形电极焊接、微组装涂胶等工艺,具备从小批量生产到大批量生产的可扩展性和灵活性后工序及组装
微组装复杂装配的解决方案,环形电极焊接、微组装涂胶等工艺,具备从小批量生产到大批量生产的可扩展性和灵活性后工序及组装 后工序及组装功能性表面强化、定制化外观工艺及全流程增值开发服务包装与灭菌
后工序及组装功能性表面强化、定制化外观工艺及全流程增值开发服务包装与灭菌 包装与灭菌全面的包装服务:包装设计与开发、工艺验证、灭菌处理和包装测试等自动化
包装与灭菌全面的包装服务:包装设计与开发、工艺验证、灭菌处理和包装测试等自动化 自动化全流程自动化解决方案,推动生产效率飞跃
自动化全流程自动化解决方案,推动生产效率飞跃 - 解决方案
- 新闻与活动
- 加入美好